自组织是指大量个体相互作用自发涌现出大规模集群结构和模式的现象,具有整体大于其组成部分之和的特性。自组织现象存在于广泛的时空尺度,例如生命就是从无机物分子的集合中涌现。近年来科学家发现,可以通过限制自组织单元的方法影响甚至控制自组织过程。限制可以作为一种工具,通过利用自组织系统与其限制特性之间的反馈控制策略,引导集群现象的涌现。本文综述了通过限制引导自组织这一活跃的跨学科领域,并指出其面临的重要研究挑战。
研究领域:自组织,群体行为,涌现
Nuno Araújo et al. | 作者
刘泽 | 译者
梁金 | 审校
邓一雪 | 编辑
论文题目:
Steering self-organisation through confinement
http://arxiv.org/abs/2204.10059
自组织(self-organisation)是一种由小型个体单元在时空结构上彼此交互从而自发产生的涌现(emergence)行为。在不同的多尺度系统与科学学科都可以找到自组织的相关例子,如物理学、材料学、机器人学、生物学以及地球物理学与天文学。当下研究的重点是如何通过限制(confinement)来影响与控制自组织行为。限制产生于与边界的相互作用中,并能对自组织行为产生促进或者抑制的功能,这将成为在时空中促进涌现行为产生或者抑制群集现象的新方法。在此,我们提出了一种针对未来相关研究的通用架构,并检验了限制在自组织中的作用,同时指出,解决限制在科学原理方面的重大挑战将有巨大科技潜力。这个通用的架构不但可以更快地加深人们对自组织的认识,而且可以促进产生创新的方法用限制来引导自组织。例如,在机敏材料的研制、生物医学中的组织工程,及群体管理中该架构都能产生重要作用。
从分子聚集[1]到动物群体[2]或是人类群体[3,4],从微泳粒子(microswimmers)[5]到微粒材料[6]与机器人集群[7],在广泛的时空尺度中都可以找到自组织系统的例子[8,9]。作为现代研究的一个领域,自组织的相关理念在20世纪就已经崭露头角[10],其定义为,在时空中由于许多个体的相互作用,从而自发产生具有大规模集群结构和模式的涌现行为[8,9],例如分子、胶粒、细胞、动物、机器人、行人甚至天体都可能产生自组织行为。这些个体在尺寸、形状、结构与功能高度不同(在生物系统中这是常见的),或是高度相同(在典型的合成系统)。这些个体可能十分活跃(例如分子马达(molecular motors)、细胞、动物、行人)或者不活跃(例如胶体、微粒物质、行星),这取决于它们是否可以将有效能转换为做功。
自组织有两个关键点值得重点介绍:第一,自组织结构的尺寸远远大于其组成单元的尺寸。第二,自组织结构产生了远超其组成单元的性能和功效。在大规模集群中出现的非平凡、非简单叠加的特点是自组织课题如此吸引人的原因。一方面,它捕捉了复杂行为如何从简单个体发展与演化得到的,例如,生命本身就从无机物分子的集合中涌现[11]。另一方面,这为材料科学家和系统科学家提供了灵感,他们旨在模仿这种自发的复杂性,用来提高人工材料与设备[12]。
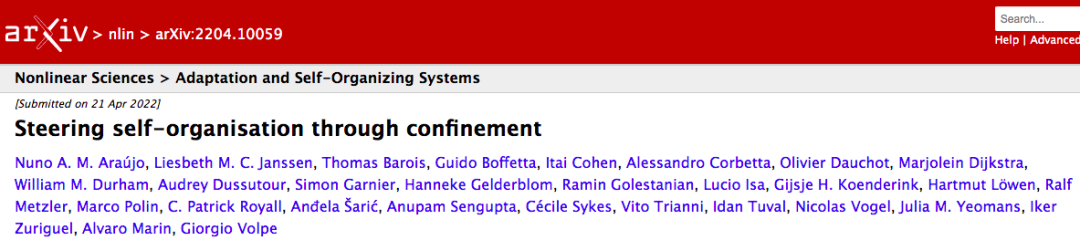
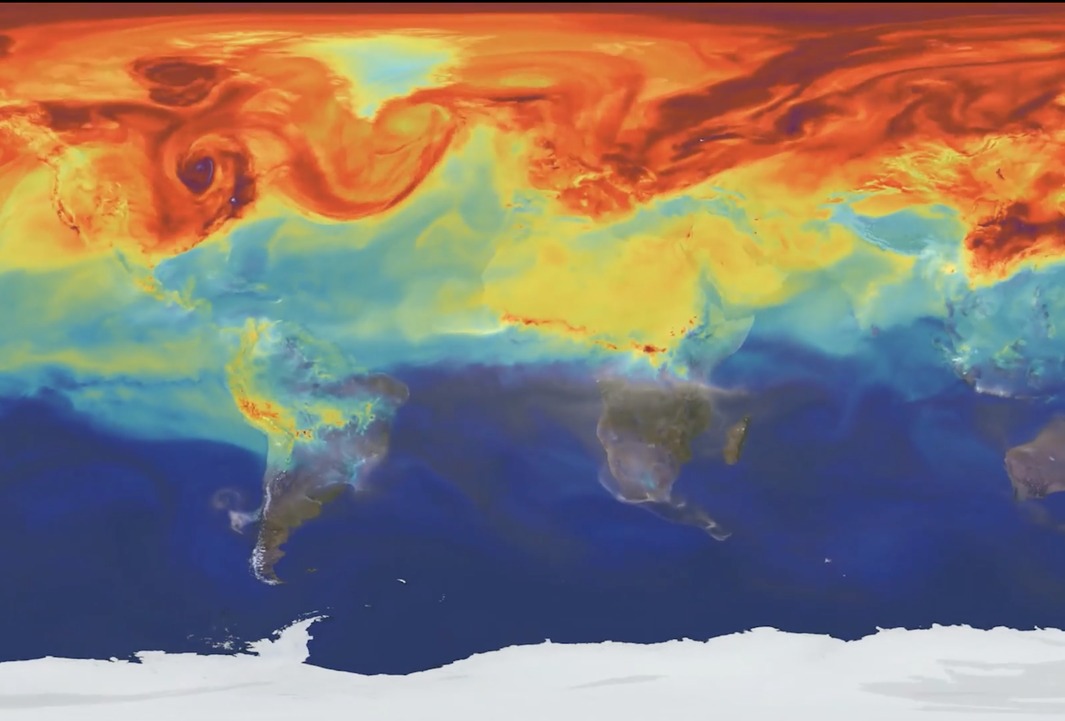
近年来,显而易见的是,可以通过限制单元的方法影响甚至控制自组织过程(图1)。这些限制行为可能来自表面、界面、场、势能、流,甚至在动物群体或人群动力学中来自无形的心理因素。[13] 因此,我们可以将自组织中的限制定义为:在给定时刻,导致个体限制在特定区域,导致涌现或者抑制集群的几乎任何事物。受限制性影响的自组织系统的种类很多,其尺度规模跨越的范围十分巨大(图2),从活细胞内被分子马达驱动的丝状体(filament)[14],到被地球大气圈限制的宏观相干流结构的涌现[15],再到黑洞引力拉扯下整个星系的形成[16]。虽然限制并不是系统形成自组织的必要条件[17],但可以作为自组织的催化剂或者抑制剂发挥重要作用。从这个方面而言,限制在自组织中最有前途的应用之一,是作为研究人员或工程师手中的控制器,调节集群现象的涌现。如在表面分子传感器[18]、组织工程支架[19]、利用物理屏障管理人群策略[20]等设计中,都可以发现这一原理的应用。
本文认为,限制可以作为一种工具,通过利用自组织系统与其限制特性之间的非平凡反馈控制策略,积极引导自组织行为。这将有助于对生物系统中的自组织行为有更深刻的理解,并指导开发控制人造系统中自组织行为的创新策略。为了实现这个目标,需要跨学科的共同努力。到目前为止,在限制意义下对理解和控制自组织做出的努力基本集中在具有特殊时空尺度的特定系统。然而,在多尺度系统与学科中发现了许多类似的问题和技术挑战,首先需要系统地解决这些问题,才能充分发挥限制在引导自组织行为中的潜力。为了提出一种通用的途径去解决这个问题,本文首先定义了一种统一的语言,讨论限制在自组织及其控制中的作用。然后,本文确定最相关的科学挑战,并列出解决问题需要的概念及技术要求。
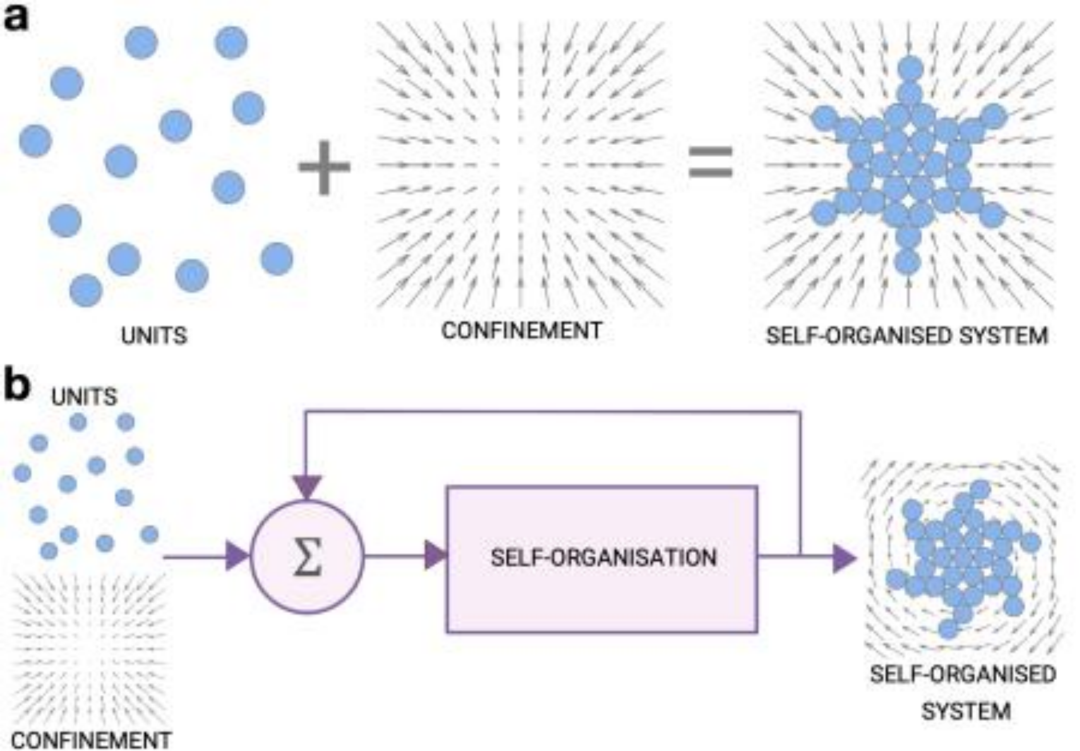
图1. 通过限制自组织单元形成的涌现结构。(a) 自组织是大规模单元形成的涌现行为。限制可以在自组织系统中发挥促进(如图所示)或者抑制作用。图中箭头代表作用在个体上的外部力场。(b) 通过限制来引导自组织系统,这就要求对反馈控制进行编码,使得个体或是被限制元素(输入)适应并与目标自组织系统(输出)共同演化。在图表中,可以看出外部力场(限制)对添加给输入的控制信号(反馈控制环)做出响应,变化以包含一个旋转。由此产生的自组织模式与a中不同。
我们首先深入讨论限制如何影响自组织。对于没有限制条件下形成的自组织系统(如表面活性剂分子在溶液中形成囊泡[24]),限制的存在可以破坏自组织,或导致替代结构和模式的形成(如表面形成的单分子层表面活性剂[24])。尽管如此,对于其他缺少限制不会形成自组织的系统(如一个活细胞的绝大部分细胞器[25]),限制是自组织涌现的一个前提条件(如通过细胞膜将细胞的内部与外界分隔开[26])。
更具体地说,限制可以有很多方式影响与引导自组织行为:它可以直接影响个体的平移和旋转自由度;它可以改变个体间交互的性质与强度,或引入新的交互;它可以限制交互个体的数量与类型;它可以改变自组织系统的相空间与能量景观(energy landscape);它可以改变个体间的交互率或交互顺序,平行反应的概率;最后,它还支持跨尺度个体间的交互。
我们可以引入几种非互斥的定义,根据限制的来源和性质对其进行分类:
-
物理限制 vs 有效限制。物理(physical)限制是指物理障碍的存在限制了系统可用的相空间(如细胞的柔性膜[2],或微泳粒子[28]、机器人[29]或行人[4]的刚性壁);相比之下,有效(effective)限制源于一个表观或虚拟的边界,由具有某种内在能力(intrinsic capability)的单元感知到(如细菌[30]或蚁群[31]的化学痕迹,胶体粒子的力场[32],微泳粒子消耗资源量随时间的变化 [28],动物和机器人的通讯范围[33],限制地球大气产生湍流的引力场[15],或者使星系聚集在一起的黑洞的引力场[16])。
-
硬边界 vs 软边界。硬边界不受自组织系统的动力学(如固体墙[34]的情况)影响,软边界则可以变形、重塑、适应并演化以响应自组织过程的动力学(就像灵活的细胞膜[35]或流体界面[36]的情况),因此,在单元和限制边界之间存在一种反馈机制。
-
静态限制 vs 动态限制。静态限制在时间上是不变的(例如,用于微泳粒子的微流体室壁(microfluidic chamber)[37],或用于限制活性颗粒物质[34]的板);相反,动态限制随时间而变化(例如,随时间变化的化学梯度作为组织中细胞群的限制场[38],或社会动物所依赖的历史时间线,如蚂蚁沿着其同伴之前走过的路径[31])。
-
正向强化 vs 负向强化。正向(positively)和负向(negatively)强化可以指示由于限制的存在,一些情形下自组织形成过程被增强(例如通过微生物群体感应(quorum sensing)中的自诱导物 [30] 或在组织形成与增生中的化学梯度[39]),一些情形下自组织过程被破坏(例如由于多孔介质,结晶过程会消退[40])。
-
外部强化 vs 自我强化。最后,限制通常被认为是一种外部特征,即不属于自组织系统。然而,在某些领域(例如在活性胶体、群居动物和集群机器人的研究中),自限制(self-imposed confinement)的概念被广泛接受,来描述通过内部反馈产生群体动力学的边界的情况(例如,像蚂蚁这样的群居动物对路径形成的感知线索 [31])。这在图2的顶部有说明,并促进了一种完全不同类型的限制。
通过限制获取对自组织的控制,需要科学界利用上面提到的更复杂的限制形式,利用有效、软、动态及自我强化边界,创建在外部或内部实施的反馈机制,引导自组织系统中集群行为的涌现或抑制(图2)。
图2. 不同约束条件下,不同尺度的自组织系统。该图包含了在自然界和人工系统中,发生在不同空间(时间)尺度下受到不同限制产生的自组织实例。横轴代表自组织单元的尺寸,从分子尺度到天文尺度。纵轴代表基于其复杂性或当前缺乏相应了解(划分可能不“科学”)划分的限制条件类型。在图的底部,为了更简便、更好地理解限制的形式,用蓝色阴影突出显示,包括外部边界(如壁(walls)、界面和势能)。在图的顶部,单独列出一种特殊的限制类型,虽然对这个限制类型了解很少,但其在引导自组织行为上有很大的潜力。这些不同类型限制包括自组织单元与限制特征之间的反馈控制环。(如在微生物生物膜形成前的群体感应中[21],在蚁群建造桥梁等结构的信息交换中[22],在原行星形成的自引力中[23])。
开发通过限制引导自组织的工具,要求我们对系统、尺度、相应学科有更深刻的了解,了解限制在时空中如何促进或抑制集群模式的涌现。我们已经确定了五个协同领域,需要更进一步的研究来推动其发展:普遍性(universality)、异质性(heterogeneity)、层级性(hierarchy)、互惠性(reciprocity)、限制的设计。虽然普遍性和异质性是研究自组织面临的共同难题,但本文主要讨论限制。
普遍性:旨在研究一个系统中观察到的模式能否推广到其他系统、尺度、学科。本质上,限制将特征(长度或时间)尺度引入了自组织进程,这可能潜在影响跨尺度的普遍性。尽管如此,研究在什么条件下可以将某个系统中观测到的特殊模式推广到其他系统与学科,是开发可控模型来研究如何通过限制引导自组织的关键。
异质性:设法解决单元(如在形态发生[41]、细胞分化和癌症细胞[42]或多分散的胶体[43])或限制(如由多孔材料诱导的异质性流和化学物质分布[44])的变化如何影响群体行为的涌现。特别是,时间和空间中限制的异质性可以用来影响自组织单元(如通过促进它们的分离或聚集[45]),反之亦然,限制也可以用来触发自组织系统中异质性的涌现(如促进细胞分化[42])。
层级性:当在特定尺度下的限制决定更大长度尺度的单元时,自组织有层次性地发生(图3)。例如在生物系统中,分子(单元)在被细胞膜限制的细胞内进行自组织 [46]。当细胞本身被细胞外基质限制而形成组织和器官时,它们也可以成为单元 [47]。组织和器官构成生物体,这些生物体可以通过感官和感知反馈,进一步形成羊群、牛群、鱼群 [48]。这些动物群体可以受当地地理分布限制而形成完整生态系统 [49]。在这些层级结构中,不同尺度的限制元素调节从小尺度到大尺度的双向交互和信息流动,反之亦然。例如,在生物学中,细胞膜是细胞内自组织的关键限制实体,但同时它将细胞定义为组织和器官的多细胞组织的单元,从而使复杂的功能得以涌现。重要的是,由于来自周围组织[50]和细胞内部的机械和化学刺激,细胞膜的形状和化学成分不断演化,从而成为不同尺度之间反馈的中介。这里的首要关键挑战是阐明、测量和模拟不同尺度上的限制如何(以及何时)调节或分离不同尺度之间的交流和相互依赖。
图3. 生物中受限制下的层级自组织实例。从分子到形成组织的层级过程,经历了大分子、细胞器、细胞的形成。在每个阶段,由于不同类型的限制,上一阶段完成自组织的结构将成为下一阶段自组织中的组成单元,这里仅在分子、细胞与组织尺度介绍。限制的来源包括,例如物理边界、机械力(F)、化学梯度。生物系统中复杂功能的涌现依赖这种层级结构。
互惠性:可以定义为单元和限制之间形成动态反馈回路,提高自组织系统在变化环境条件下的适应性、响应能力甚至演化。创伤愈合和组织再生中的细胞-基质相互作用就是一个例子[51],细胞外基质限制细胞,迫使它们采用特定的形态。接下来机械信号转导(mechanotransduction)可以诱导细胞开始分泌与周围细胞外基质匹配的胶原蛋白,进一步促进细胞组织形成。理解自组织单元和限制之间的相互作用能够解决一些基本问题(例如,生命是限制的产物或是相反的情况?),并且定义设计规则来利用限制引导自组织。
限制的设计:最后的挑战是识别和执行明确的设计规则,在不同限制条件下,预测特定单元的涌现模式(正向设计),或优化单元以获得目标的时空结构(反向设计)。为了实现最优控制,需要在单元和限制元素中动态编码信息,以产生复杂、可适应的反馈机制。生物系统特别擅长编码信息(例如通过DNA和RNA)和动态利用限制来创造功能(例如,将DNA封装在细胞核内的染色体中,或在细胞中组装和分出功能区隔,如溶酶体或无膜细胞器)。我们还有广阔的空间以进一步开发人造系统来模拟这种生物复杂性并利用技术应用的涌现,例如为生物医学开发可编程材料和智能设备[12]或人群管理[20]。
上述讨论强调了未来研究的几个途径,要解决这些问题需要多个概念与技术进展。由于研究方法和技术通常适用于特定的系统,我们预期在通过限制引导自组织的背景下,不同尺度和学科将面临以下开放的技术挑战。
首先,我们必须开发先进的工具来精确地描述约束、单元之间的相互作用和涌现的结构。在实验上,约束的性质和强度并不总是容易识别或量化的,对于有效边界(例如化学梯度)、移动边界(由于时间依赖性)和自我施加的限制形式(本质上很难定义和探测)来说尤其具有挑战性。此外,测量行为甚至可能改变限制元素本身的性质,正如生物学版本的玻尔互补原理[52]所预测的那样。同样,测量这些单元之间的相互作用也可能带来重大挑战:例如,在组织中,细胞-细胞相互作用受到生化和机械信号通路的复杂相互作用的影响,甚至受到周围培养基[51]施加的限制;在人群和动物群体中,相互作用受到难以量化的心理和认知因素的影响,特别是考虑到个体之间的内在异质性[2,53]。最后,依靠外部实验来动态探测正在涌现的自组织结构是十分困难的:例如,由于边界的部分或完全不透明,使用光学显微镜实时成像在体内可能会有问题,以及限制本身会成为提取自组织系统信息的障碍[54];在胶体系统中,相互作用虽然在体积上可以很好地测量和理解,但在液体界面[36]处却很少被理解;体内测量也可能特别困难,因为用于探测系统的技术可能很快变得具有强烈的侵袭性,从而影响系统本身情况(例如荧光显微镜成像[55]引起的光毒性和漂白)。
其次,为了更深入地理解如何通过限制来引导自组织,我们必须学会识别和利用给定尺度和跨尺度的关键物理特征。值得注意的是,在层次约束和互惠的背景下,在完全理解不同尺度的完整相互作用前,首先必须了解影响信息流的相关量的意义(如PH值、浓度、机械力、流体速度、化学梯度、弹性等),并且能够测量这些量。这里,新的多尺度和粗粒度模型将特别关键,其开发应该与实验工作密切协同以便验证。更一般地,我们必须努力开发足够简单和易于控制的实验和模型以便于科学解释,但它们也必须足够精确,以便指导在现实条件下捕获观察到的相关现象。如果我们想要使用这些模型来预测不同类型的限制以及特定单元如何引导自组织,这就显得尤为必要。
最后,在限制条件下进行设计时,我们必须使单元和边界同时具有信息编码和处理的自由度(不受限制的个体),使自适应反馈机制成为可能。根据研究的尺度和系统,信息编码单元和限制的制造可以通过诸如基因工程、纳米和微细制造、3D打印或时变场等技术来实现。一个关键的技术挑战是对小型化的强烈需求(如精确医疗等特定应用的需求),这将限制我们在未来几年设计和控制更小尺度的自组织单元和限制的方式。最后,机器学习领域的快速发展,对指导相应的设计与探索有着巨大的潜力,无论是新材料设计(单元和边界),还是在空间和时间中发现新的自组织结构 [56]。
总之,通过限制来引导自组织是一个非常活跃和快速发展的研究领域,本质上是多学科交叉的。为了推动这一领域的发展,致力于自组织的科学社区应该越来越多地利用来自不同领域和学科的专家基于共同猜想、理论和实验方法产生的思想(例如,物理科学和生命科学之间,在合成系统和自然系统之间,在小尺度和大尺度之间)。这种跨领域交流是不容易的,因为它需要共同的语言和在关键问题和目标上达成一致。当然,前面的道路仍然艰难,需要共同采取许多步骤,使更广泛的科学社区团结起来,以协同的方式推动领域发展。本文朝这个方向迈出了第一步。我们希望它将成为一个推动力,使更多科学人员加入这一集体努力,共同迎接通过限制引导自组织这一可能性带来的跨领域、长度与时间尺度的令人振奋的挑战。
[1] Whitesides, G.M., Mathias, J.P., Seto, C.T.: Molecular self-assembly and nanochemistry: a chemical strategy for the synthesis of nanostructures. Science 254(5036), 1312–1319 (1991)
[2] Moussaïd, M., Garnier, S., Theraulaz, G., Helbing, D.: Collective infor- mation processing and pattern formation in swarms, flocks, and crowds. Top. Cogn. Sci. 1(3), 469–497 (2009)
[3] Moussaïd, M., Helbing, D., Theraulaz, G.: How simple rules determine
pedestrian behavior and crowd disasters. Proc. Natl. Acad. Sci. U.S.A. 108(17), 6884–6888 (2011)
[4] Echeverría-Huarte, I., Nicolas, A., Hidalgo, R.C., Garcimartín, A.,
Zuriguel, I.: Spontaneous emergence of counterclockwise vortex motion in assemblies of pedestrians roaming within an enclosure. Scientific Reports 12(1), 1–9 (2022)
[5] Bechinger, C., Di Leonardo, R., Löwen, H., Reichhardt, C., Volpe, G.,
Volpe, G.: Active particles in complex and crowded environments. Rev. Mod. Phys. 88, 045006 (2016)
[6] Silbert, L.E., Grest, G.S., Plimpton, S.J., Levine, D.: Boundary effects and self-organization in dense granular flows. Phys. Fluids 14(8), 2637–2646 (2002)
[7] Oh, H., Shirazi, A.R., Sun, C., Jin, Y.: Bio-inspired self-organising multi-
robot pattern formation: A review. Robot. Auton. Syst. 91, 83–100 (2017)
[8] Whitesides, G.M., Grzybowski, B.: Self-assembly at all scales. Science 295(5564), 2418–2421 (2002)
[9] Camazine, S., Deneubourg, J.-L., Franks, N.R., Sneyd, J., Theraulaz,G., Bonabeau, E.: Self-organization in Biological Systems. Princeton University Press, Princeton, New Jersey (2001)
[10] Prigogine, I.: Etude thermodynamique des phénomènes irreversible. Bull.Acad. Roy. Blg. Cl. Sci. 31, 600–606 (1945)
[11] Karsenti, E.: Self-organization in cell biology: a brief history. Nat. Rev,
Mol. Cell Biol. 9(3), 255–262 (2008)
[12] Grzybowski, B.A., Fitzner, K., Paczesny, J., Granick, S.: From dynamic
self-assembly to networked chemical systems. Chem. Soc. Rev. 46(18), 5647–5678 (2017)
[13] Sieben, A., Schumann, J., Seyfried, A.: Collective phenomena in crowds—where pedestrian dynamics need social psychology. PLoS one 12(6), 0177328 (2017)
[14] Opathalage, A., Norton, M.M., Juniper, M.P., Langeslay, B., Aghvami,
S.A., Fraden, S., Dogic, Z.: Self-organized dynamics and the transition to turbulence of confined active nematics. Proc. Natl. Acad. Sci. U.S.A. 116(11), 4788–4797 (2019)
[15] Boffetta, G., Ecke, R.E.: Two-dimensional turbulence. Annu. Rev. Fluid
[16] Kravtsov, A.V., Borgani, S.: Formation of galaxy clusters. Annu. Rev.
Astron. Astrophys. 50, 353–409 (2012)
[17] Vicsek, T., Zafeiris, A.: Collective motion. Phys. Rep. 517(3-4), 71–140
[18] Taylor, A.B., Zijlstra, P.: Single-molecule plasmon sensing: current status and future prospects. ACS Sens. 2(8), 1103–1122 (2017)
[19] Mafalda D. Neto, J.F.M. Mariana B. Oliveira: Microparticles in contact
with cells: From carriers to multifunctional tissue modulators. Trends Biotechnol. 37, 1011–1028 (2019)
[20] Feliciani, C., Zuriguel, I., Garcimartín, A., Maza, D., Nishinari, K.:
Systematic experimental investigation of the obstacle effect during non- competitive and extremely competitive evacuations. Sci. Rep. 10(1), 1–20
[21] Miller, M.B., Bassler, B.L.: Quorum sensing in bacteria. Annu. Rev.
Microbiol. 55(1), 165–199 (2001)
[22] McCreery, H.F., Gemayel, G., Pais, A.I., Garnier, S., Nagpal, R.: Hystere- sis stabilizes dynamic control of self-assembled army ant constructions. Nat. Commun. 13(1), 1–13 (2022)
[23] Aschwanden, M.J., Scholkmann, F., Béthune, W., Schmutz, W., Abra-
menko, V., Cheung, M.C.M., Müller, D., Benz, A., Chernov, G., Kritsuk, A.G., Scargle, J.D., Melatos, A., Wagoner, R.V., Trimble, V., Green, W.H.: Order out of Randomness: Self-Organization Processes in Astro- physics. Space Sci. Rev. 214(2), 55 (2018)
[24] Doi, M.: Soft Matter Physics. Oxford University Press, Oxford, United
[25] McCusker, D.: Cellular self-organization: generating order from the abyss. Mol. Biol. Cell 31(3), 143–148 (2020)
[26] Sezgin, E., Levental, I., Mayor, S., Eggeling, C.: The mystery of membrane organization: composition, regulation and roles of lipid rafts. Nat. Rev. Mol. Cell Biol. 18(6), 361–374 (2017)
[27] Bashirzadeh, Y., Liu, A.P.: Encapsulation of the cytoskeleton: towards
mimicking the mechanics of a cell. Soft Matter 15(42), 8425–8436 (2019)
[28] Lavergne, F.A., Wendehenne, H., Bäuerle, T., Bechinger, C.: Group for- mation and cohesion of active particles with visual perception-dependent motility. Science 364(6435), 70–74 (2019)
[29] Scholz, C., Engel, M., Pöschel, T.: Rotating robots move collectively and
self-organize. Nat. Commun. 9(1), 1–8 (2018)
[30] Mukherjee, S., Bassler, B.L.: Bacterial quorum sensing in complex and
dynamically changing environments. Nat. Rev. Microbiol. 17(6), 371–382 (2019)
[31] Czaczkes, T.J., Grüter, C., Ratnieks, F.L.: Trail pheromones: an integra-
tive view of their role in social insect colony organization. Annu. Rev. Entomol. 60, 581–599 (2015)
[32] Ebert, F., Dillmann, P., Maret, G., Keim, P.: The experimental realization
of a two-dimensional colloidal model system. Rev. Sci. Instrum. 80(8), 083902 (2009)
[33] Rubenstein, M., Cornejo, A., Nagpal, R.: Programmable self-assembly in
a thousand-robot swarm. Science 345(6198), 795–799 (2014)
[34] Briand, G., Schindler, M., Dauchot, O.: Spontaneously flowing crystal of self-propelled particles. Phys. Rev. Lett. 120(20), 208001 (2018)
[35] Tsai, F.-C., Koenderink, G.H.: Shape control of lipid bilayer membranes by confined actin bundles. Soft Matter 11(45), 8834–8847 (2015)
[36] Bradley, L.C., Chen, W.-H., Stebe, K.J., Lee, D.: Janus and patchy col-loids at fluid interfaces. Curr. Opin. Colloid Interface Sci. 30, 25–33 (2017)
[37] Sharan, P., Nsamela, A., Lesher-Pérez, S.C., Simmchen, J.: Microfluidics for microswimmers: Engineering novel swimmers and constructing swim- ming lanes on the microscale, a tutorial review. Small 17(26), 2007403 (2021)
[38] Kerszberg, M., Wolpert, L.: Specifying positional information in the embryo: looking beyond morphogens. Cell 130(2), 205–209 (2007)
[39] Michailidi, M.R., Hadjivasiliou, Z., Aguilar-Hidalgo, D., Basagiannis, D.,Seum, C., Dubois, M., Jülicher, F., Gonzalez-Gaitan, M.: Morphogen gradient scaling by recycling of intracellular dpp. Nature 602, 287–293 (2022)
[40] Alba-Simionesco, C., Coasne, B., Dosseh, G., Dudziak, G., Gubbins, K.,
Radhakrishnan, R., Sliwinska-Bartkowiak, M.: Effects of confinement on freezing and melting. J. Condens. Matter Phys. 18(6), 15 (2006)
[41] Teague, B.P., Guye, P., Weiss, R.: Synthetic morphogenesis. Cold Spring
Harb. Perspect. Biol. 8(9), 023929 (2016)
[42] Baron, C.S., van Oudenaarden, A.: Unravelling cellular relationships dur-
ing development and regeneration using genetic lineage tracing. Nat. Rev. Mol. Cell Biol. 20(12), 753–765 (2019)
[43] Abraham, S.E., Bhattacharrya, S.M., Bagchi, B.: Energy landscape, antiplasticization, and polydispersity induced crossover of heterogeneity in supercooled polydisperse liquids. Phys. Rev. Lett. 100(16), 167801 (2008)
[44] de Anna, P., Pahlavan, A.A., Yawata, Y., Stocker, R., Juanes, R.: Chemo- taxis under flow disorder shapes microbial dispersion in porous media. Nat. Phys. 17(1), 68–73 (2021)
[45] Aref, H., Blake, J.R., Budiši ć, M., Cardoso, S.S.S., Cartwright, J.H.E.,
Clercx, H.J.H., El Omari, K., Feudel, U., Golestanian, R., Gouillart,
E., van Heijst, G.F., Krasnopolskaya, T.S., Le Guer, Y., MacKay, R.S., Meleshko, V.V., Metcalfe, G., Mezi ć, I., de Moura, A.P.S., Piro, O., Speetjens, M.F.M., Sturman, R., Thiffeault, J.-L., Tuval, I.: Frontiers of chaotic advection. Rev. Mod. Phys. 89, 025007 (2017)
[46] Merino-Salomón, A., Babl, L., Schwille, P.: Self-organized protein pat-
terns: The mincde and parabs systems. Curr. Opin. Cell Biol. 72, 106–115 (2021)
[47] Chaudhuri, O., Cooper-White, J., Janmey, P.A., Mooney, D.J., Shenoy,
V.B.: Effects of extracellular matrix viscoelasticity on cellular behaviour. Nature 584(7822), 535–546 (2020)
[48] Ballerini, M., Cabibbo, N., Candelier, R., Cavagna, A., Cisbani, E., Giardina, I., Lecomte, V., Orlandi, A., Parisi, G., Procaccini, A., et al.: Interaction ruling animal collective behavior depends on topological rather than metric distance: Evidence from a field study. Proc. Natl. Acad. Sci. U.S.A. 105(4), 1232–1237 (2008)
[49] Gude, S., Pinçe, E., Taute, K.M., Seinen, A.-B., Shimizu, T.S., Tans, S.J.:
Bacterial coexistence driven by motility and spatial competition. Nature 578(7796), 588–592 (2020)
[50] Balasubramaniam, L., Mège, R.-M., Ladoux, B.: Active nematics across
scales from cytoskeleton organization to tissue morphogenesis. Curr. Opin. Genet. Dev. 73, 101897 (2022)
[51] Foolen, J., Wunderli, S.L., Loerakker, S., Snedeker, J.G.: Tissue alignment enhances remodeling potential of tendon-derived cells – lessons from a novel microtissue model of tendon scarring. Matrix Biol. 65, 14–29 (2018)
[52] Bohr, N.: Light and life. Nature 131, 457–459 (1933)
[53] von Sivers, I., Templeton, A., Künzner, F., Köster, G., Drury, J., Philip-
pides, A., Neckel, T., Bungartz, H.-J.: Modelling social identification and helping in evacuation simulation. Saf. Sci. 89, 288–300 (2016)
[54] Yoon, S., Kim, M., Jang, M., Choi, Y., Choi, W., Kang, S., Choi, W.:
Deep optical imaging within complex scattering media. Nat. Rev. Phys. 2(3), 141–158 (2020)
[55] Icha, J., Weber, M., Waters, J.C., Norden, C.: Phototoxicity in live flu-
orescence microscopy, and how to avoid it. BioEssays 39(8), 1700003 (2017)
[56] Wei, J., Chu, X., Sun, X.-Y., Xu, K., Deng, H.-X., Chen, J., Wei, Z., Lei,
M.: Machine learning in materials science. InfoMat 1(3), 338–358 (2019)
集智斑图顶刊论文速递栏目上线以来,持续收录来自Nature、Science等顶刊的最新论文,追踪复杂系统、网络科学、计算社会科学等领域的前沿进展。现在正式推出订阅功能,每周通过微信服务号「集智斑图」推送论文信息。扫描下方二维码即可一键订阅:

点击“阅读原文”,追踪复杂科学顶刊论文